震撼! FDA上市"廣譜"抗癌藥治癒率75%
美國FDA批准了larotrectinib(LOXO-101)的上市,用於治療患有NTRK基因融合的局部晚期或轉移性實體瘤的成人和兒童患者,治療包括肺癌、甲狀腺癌、結腸癌等17種癌症。

2018年10月歐洲腫瘤內科學會年會(ESMO)在德國召開,Larotrectinib又公布了一組“神乎奇蹟”的臨床數據:54位NTRK融合的患者,使用Larotrectinib治療後,17%的患者腫瘤完全消失,有效率高達82%。
具體如下圖:

2018年新公布的54位NTRK融合患者數據
其實,早在2017年6月的美國臨床腫瘤學會年會(ASCO)上,Larotrectinib就公布過另外55位NTRK融合患者的臨床數據,有效率高達75%,
所以,截止目前,一共有55+54=119位NTRK融合的患者用過Larotrectinib,總體有效率保持在81%,其中17%的患者腫瘤完全消失。
具體如下:
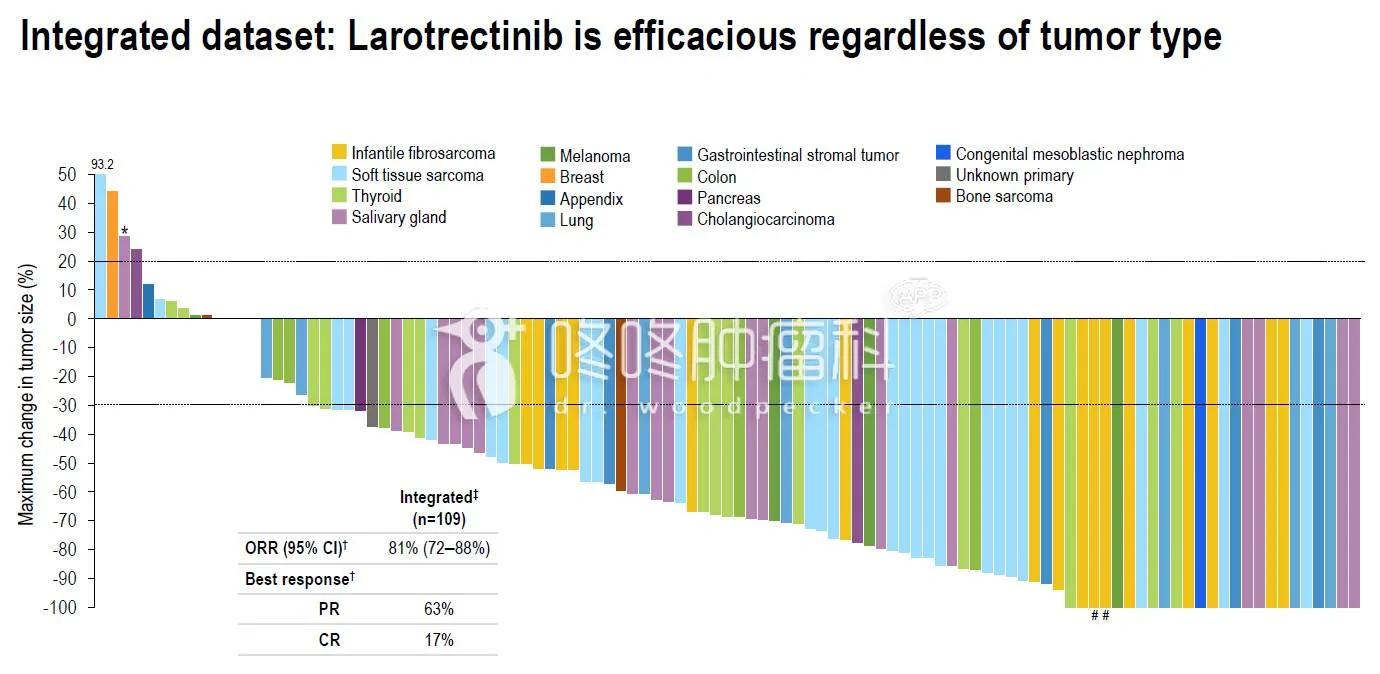
總共119位NTRK融合患者的臨床數據
Larotrectinib代號為LOXO-101,是一個針對的是NTRK1、NTRK2或者NTRK3基因融合的靶向葯,由LoxoOncology公司研發,後來德國拜耳公司跟Loxo Oncology合作,共同開發Larotrectinib藥物。
Larotrectinib適合哪些癌症患者?
Larotrectinib本質還是是一個靶向葯,針對的是NTRK1、NTRK2或者NTRK3基因融合的腫瘤患者。也就是說,凡是有這三個基因融合的患者,不限癌症類型,都可以考慮使用Larotrectinib。
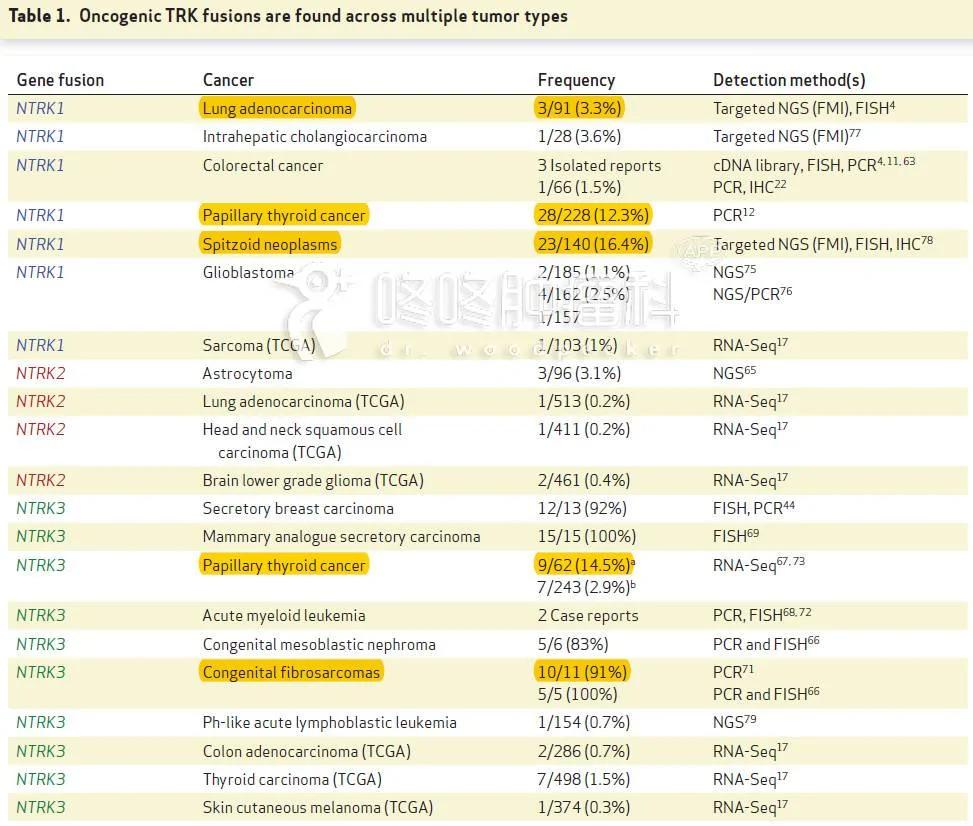
根據2015年的一份研究[3],NTRK融合常出現在先天性纖維肉瘤、先天性中胚層腎癌和分泌型乳腺癌(各90%以上)以及乳頭狀甲狀腺癌(26%)等罕見腫瘤,這些患者可以積極進行NTRK融合的檢測,概率還是很大的。
而對於國內常見的肺癌和腸癌,NTRK融合的比例比較低,分別在3.5%和1.5%。不過,對於做過多基因檢測的患者(一般是同時檢測幾百個基因),一定去看看檢測報告有沒有這個NTRK基因融合。雖然概率低,萬一碰上了,就真的中大獎了。

larotrectinib的前世今生
TRK融合是一種基因異常,指的TRK基因與其他基因融合,據估計,這種異常的發生占常見腫瘤的0.5%~1%,但在某些罕見腫瘤中所佔比例超過90%,例如唾液腺癌、某種青年型乳腺癌和嬰兒型纖維肉瘤中,TRK融合在腫瘤發生早期即出現,並在腫瘤生長和播散過程中持續存在。
不同於以往的靶向藥物,Larotrectinib是新一代具備高度特異性的口服TRK抑製劑,同時也是一款從早期開發時期開始就針對特定基因突變,而不針對特定癌症種類的廣譜腫瘤葯,可用於所有表達有原肌球蛋白受體激酶的腫瘤患者,而不是針對某個解剖位置的腫瘤,這就使得它的治療範圍非常廣。
Larotrectinib曾在2016年7月13日被FDA授予突破性藥物資格,用於TRK融合基因突變陽性的成人及兒童的不可手術切除或轉移性實體瘤。
在2017年召開的美國臨床腫瘤學會(ASCO)會議上,紀念斯隆-凱特琳癌症中心的DavidHyman博士公布了larotrectinib的早期臨床數據,數據顯示,Larotrectinib在廣泛的年齡和腫瘤類型的TRK融合癌症中,具有持久的抗腫瘤活性作用和良好的耐受性,成為了2017ASCO大會上的一匹黑馬。
時隔半年,2月新英格蘭醫學雜誌(NEJM)在線發表了larotrectinib(LOXO-101)同時進行的三項安全性和有效性研究結果,研究顯示對於年齡為4個月至76歲的患者,針對17種不同癌症治療總體反應率為75%。這三項研究包括成人I期研究,兒童I-II期研究,以及青少年和成人II期研究(NCT02122913,NCT02637687和NCT02576431)。結果顯示,無論患者的年齡或腫瘤類型如何,Larotrectinib對TRK融合陽性的癌症患者均具有明顯且持久的抗腫瘤活性。
在今年10月份舉行的2018年歐洲腫瘤醫學協會會議(ESMO2018)上,一項關於larotrectinib治療涵蓋24種獨特腫瘤類型的TRK融合癌症成人及兒童患者的臨床數據顯示,總緩解率(ORR)為80%,部分緩解率(PR)為62%、完全緩解率(CR)為18%,在補充數據集中,ORR為81%、PR為65%、CR為17%。
另值得一提的是,為了應對耐葯問題,Loxo已經開發出第二代TRK融合基因突變抑製劑LOXO-195,用於治療那些對larotrectinib產生耐藥性的患者,目前,LOXO-195也已獲得了頗為滿意的初步臨床數據,該數據此前已發表於美國癌症研究學會(AACR)旗下的《CancerDiscovery》雜誌上,通過對Larotrectinib耐葯的前2名患者治療顯示,經LOXO-195治療獲得了緩解。
FDA局長ScottGottlieb表示:“對於larotrectinib的加速批准上市,標誌著治療癌症的療法從基於人體起源組織向基於腫瘤遺傳特徵轉變的重要一步,我們現在有能力讓合適的患者在正確的時間獲得匹配藥物的治療。”
來源:綜合新聞

